01 研究背景
心脏重构是各种心血管疾病发展过程中常见的病理生理过程,但目前仍缺乏有效的干预措施。肿瘤坏死受体相关因子7(TRAF7)属于肿瘤坏死因子受体相关因子家族,在生物过程中起重要作用。先前的研究表明,TRAF7突变会导致先天性心脏缺陷和畸形。然而,TRAF7在病理性心肌肥厚发病机制中的分子机制尚不清楚。武汉大学人民医院唐其柱教授团队在Cardiovascular Research (IF 10.2)上发表文章“Cardiac tumour necrosis factor receptor-associated factor 7 mediates the ubiquitination of apoptosis signal-regulating kinase 1 and aggravates cardiac hypertrophy”,发现TRAF7是心脏肥厚过程中一个重要的调节因子,TRAF7直接与凋亡信号调节激酶-1(ASK1)相互作用,并在PE刺激下通过介导ASK1的K63连锁泛素化来促进ASK1磷酸化,进而促进心脏肥大过程中ASK1的激活和下游信号传导,表明调控TRAF7和ASK1可能是一种新的心肌肥厚治疗策略。

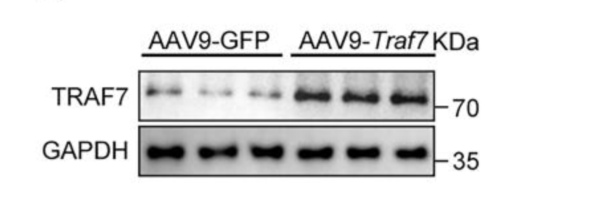
AAV9-cTNT-Traf7在小鼠心脏中过表达TRAF7

02 结果展示
1. 心脏特异性的TRAF7过表达加速心脏重构
作者发现TRAF7在实验性肥厚模型中表达升高,并能在体外促进心肌细胞肥大。为研究TRAF7的作用机制,作者用AAV9-cTNT-Traf7在小鼠心脏中过表达TRAF7,发现TRAF7的过表达加重了TAC诱导的心肌肥厚、心脏重量增加,恶化了左室收缩功能,HW/BW、LW/BW、HW/TL比值均增加。HE染色显示TAC4周后,TRAF7过表达小鼠的心肌细胞CSA显著增加。PSR检测显示TAC诱导的心脏间质纤维化和血管周围纤维化均因TRAF7过表达而加重。此外TRAF7过表达组心肌肥厚和心肌纤维化相关基因mRNA水平均显著升高。这些结果表明TRAF7过表达加速心功能障碍、心脏肥厚和心脏重构。进一步研究发现TRAF7通过促进ASK1的磷酸化来调节ASK1-JNK1/2/p38轴,进而促进心脏肥厚。
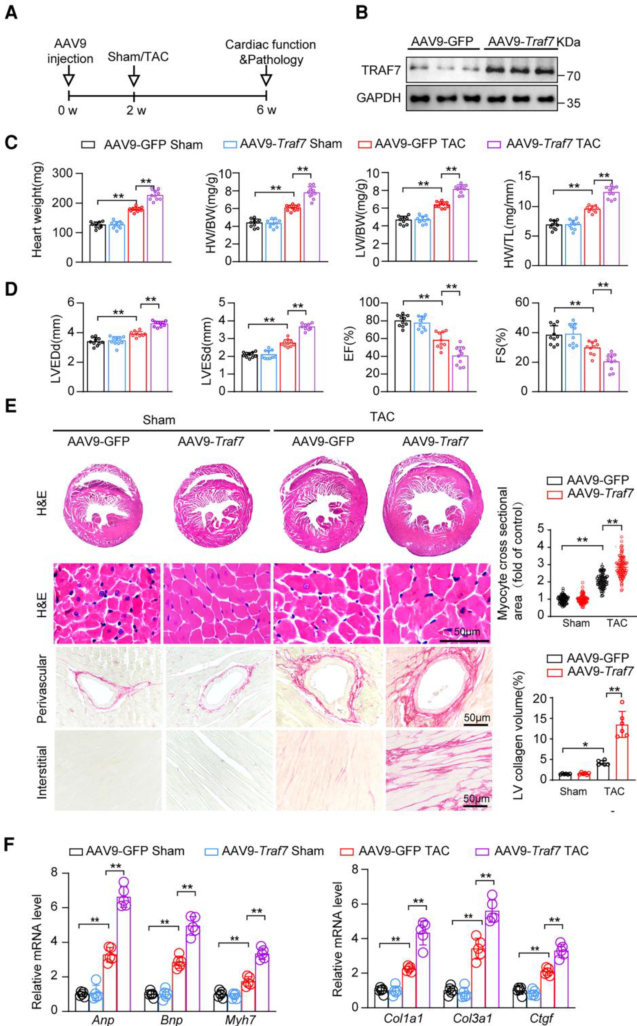
图1 心脏特异性的TRAF7过表达加速心脏重构
2. TRAF7通过促进ASK1泛素化调节ASK1的激活
作者通过IP、GST下拉、双免疫荧光染色和Co-IP等实验结果证明ASK1与TRAF7存在相互作用。由于TRAF7具有E3泛素连接酶活性,接下来作者研究了TRAF7是否通过其E3泛素连接酶活性影响ASK1的活性。研究结果表明PE明显触发了NRCM(新生大鼠心肌细胞)中ASK1泛素化,并提高了ASK1磷酸化水平,假手术或TAC手术的野生型(WT)和AAV9-Traf7小鼠的体内泛素化实验中也检测了ASK1的泛素化和磷酸化,TRAF7过表达上调ASK1的泛素化和磷酸化。此外,在过表达TRAF7的293T细胞中也观察到ASK1泛素化和磷酸化的增加,表明ASK1泛素化和磷酸化是相关的,而TRAF7可以促进这两个过程。进一步研究发现过表达TRAF7导致ASK1的k63连锁泛素化水平升高,K1064是负责TRAF7介导的Lys63连锁泛素化的泛素化位点,从而触发ASK1磷酸化活化。
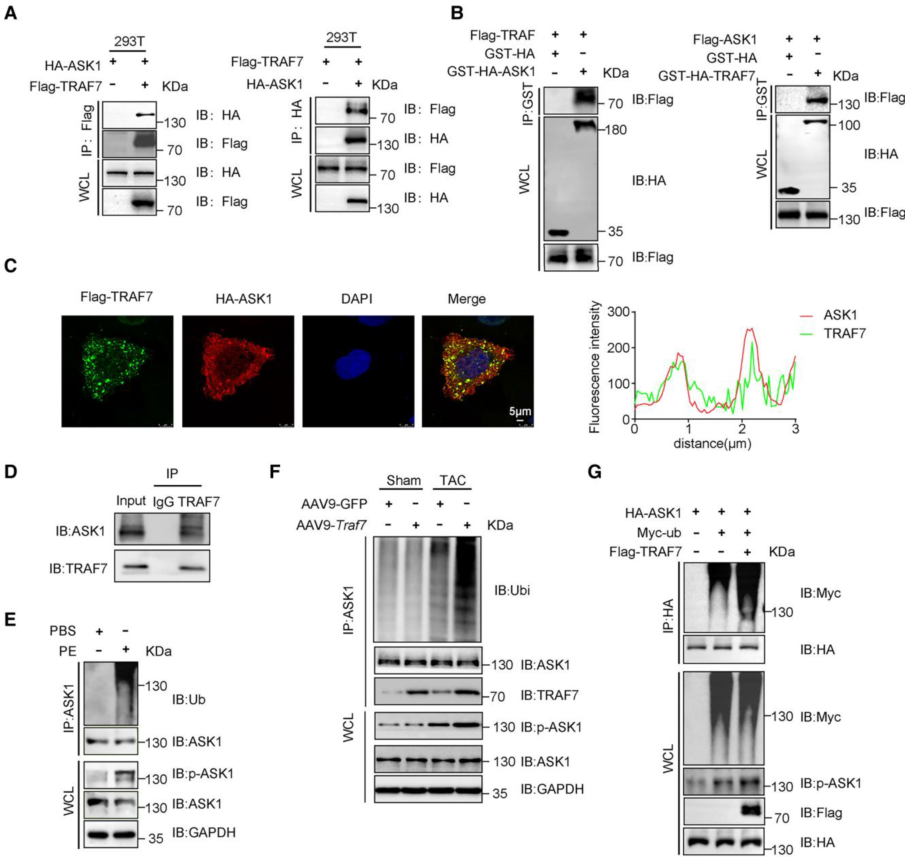
图2 TRAF7通过促进ASK1泛素化调节ASK1的激活
3. ASK1是TRAF7诱导心肌肥厚的靶点
为了进一步探讨TRAF7是否通过激活ASK1调控心肌肥大,作者在TRAF7过表达的情况下,利用ASK1特异性抑制剂GS4997抑制ASK1激活。结果显示,与PE刺激后TRAF7过表达相比,GS4997挽救了细胞的CSA,降低了TRAF7过表达上调的Anp、Bnp和Myh7 mRNA水平。此外TRAF7诱导的PE刺激后ASK1/JNK/p38轴的激活被GS4997抑制。然后作者用Ask1-CKO小鼠在体内进行了拯救实验,结果显示,Ask1-CKO能够显著拯救压力过载诱导的心脏重构,同时也能够抑制TRAF7过表达诱导的严重心脏重构。这表明在TAC诱导的心肌肥厚过程中,ASK1是TRAF7的关键下游靶点。
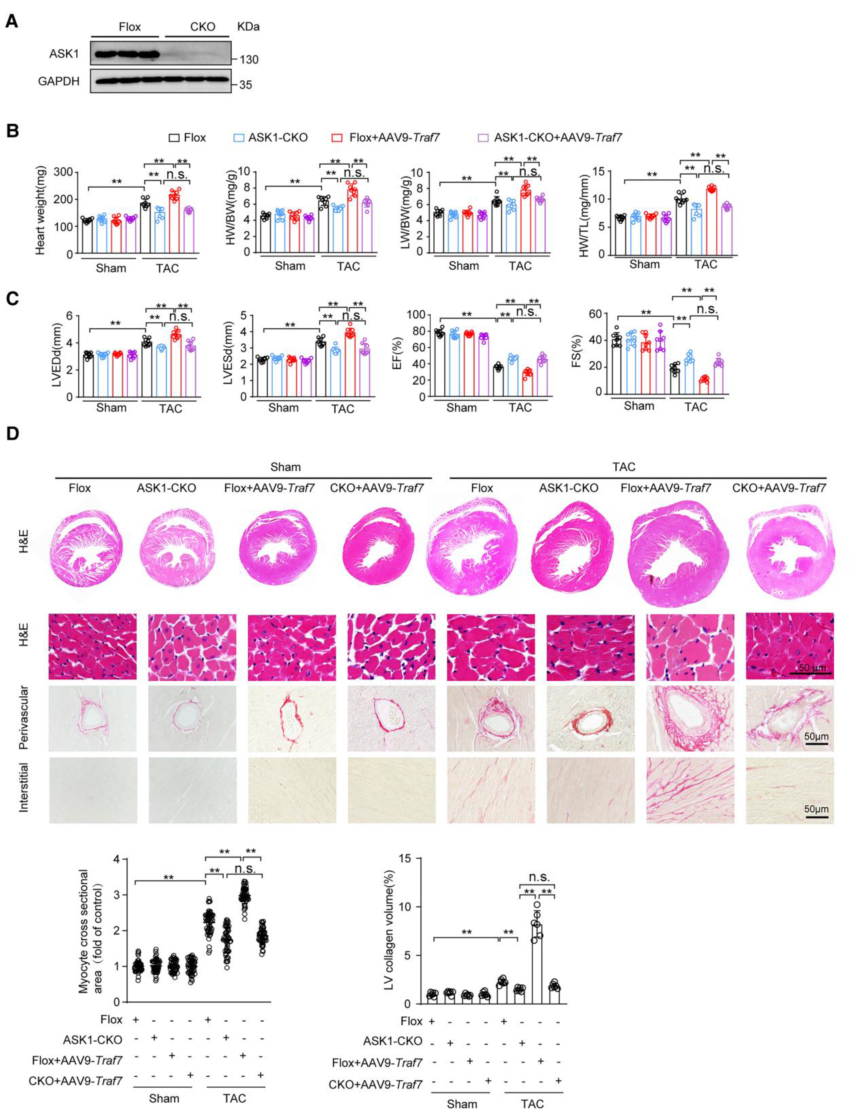
图3 ASK1是TRAF7诱导心肌肥厚的靶点
03 实验结论
本研究发现TRAF7在心脏肥厚过程中是一个重要的调节因子,TRAF7直接与ASK1相互作用,并在PE刺激下通过介导ASK1的K63连锁泛素化来促进ASK1磷酸化,进而促进心脏肥大过程中ASK1的激活和下游信号传导,调控TRAF7和ASK1可能是一种新的心肌肥厚治疗策略。
